Пептиди - це клас сполук, утворених з'єднанням кількох амінокислот за допомогою пептидних зв'язків.Вони всюдисущі в живих організмах.До теперішнього часу в живих організмах знайдено десятки тисяч пептидів.Пептиди відіграють важливу роль у регуляції функціональної активності різних систем, органів, тканин і клітин, а також у життєдіяльності, і часто використовуються у функціональному аналізі, дослідженні антитіл, розробці ліків та інших областях.З розвитком біотехнології та технології синтезу пептидів все більше і більше пептидних препаратів було розроблено та застосовано в клініці.
Існує широкий спектр модифікацій пептидів, які можна просто розділити на постмодифікацію та модифікацію процесу (з використанням модифікації похідної амінокислоти), а також модифікацію N-кінца, модифікацію C-кінца, модифікацію бічного ланцюга, модифікацію амінокислоти, модифікацію скелета, і т.д., залежно від місця модифікації (рис. 1).Будучи важливим засобом для зміни структури головного ланцюга або груп бічних ланцюгів пептидних ланцюгів, модифікація пептидів може ефективно змінювати фізичні та хімічні властивості пептидних сполук, підвищувати розчинність у воді, подовжувати час дії in vivo, змінювати їх біологічний розподіл, усувати імуногенність , зменшити токсичні побічні ефекти тощо. У цій статті представлено кілька основних стратегій модифікації пептидів та їх характеристики.
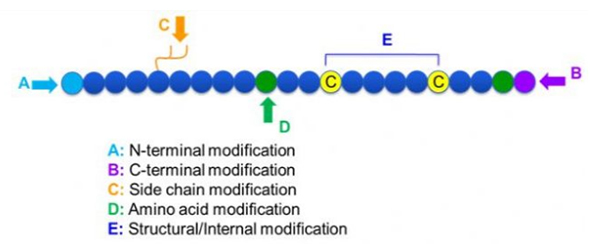
1. Циклізація
Циклічні пептиди мають багато застосувань у біомедицині, і багато природних пептидів з біологічною активністю є циклічними пептидами.Оскільки циклічні пептиди, як правило, більш жорсткі, ніж лінійні пептиди, вони надзвичайно стійкі до травної системи, можуть виживати в травному тракті та виявляють сильнішу спорідненість до цільових рецепторів.Циклізація є найбільш прямим способом синтезу циклічних пептидів, особливо для пептидів з великим структурним скелетом.Відповідно до режиму циклізації його можна розділити на тип бічного ланцюга, тип бічного ланцюга, кінцевий тип бічного ланцюга, кінцевий тип кінцевого (тип кінця до кінця).
(1) бічний ланцюг до бічного ланцюга
Найбільш поширеним типом циклізації від бічного ланцюга до бічного ланцюга є дисульфідне з’єднання між залишками цистеїну.Ця циклізація вводиться шляхом зняття захисту з пари залишків цистеїну, які потім окислюються з утворенням дисульфідних зв’язків.Поліциклічний синтез може бути досягнутий селективним видаленням сульфгідрильних захисних груп.Циклізацію можна проводити або в розчиннику після дисоціації, або на смолі перед дисоціацією.Циклізація на смолах може бути менш ефективною, ніж циклізація розчинником, оскільки пептиди на смолах не легко утворюють цикліфіковані конформації.Іншим типом циклізації бічного ланцюга є утворення амідної структури між залишком аспарагінової або глутамінової кислоти та основною амінокислотою, що вимагає, щоб захисна група бічного ланцюга могла бути вибірково видалена з поліпептиду або на смолі або після дисоціації.Третій тип бічного ланцюга - циклізація бічного ланцюга - це утворення дифенілових ефірів тирозином або п-гідроксифенілгліцином.Цей тип циклізації в природних продуктах зустрічається лише в мікробних продуктах, і продукти циклізації часто мають потенційну медичну цінність.Отримання цих сполук вимагає унікальних умов реакції, тому їх не часто використовують у синтезі звичайних пептидів.
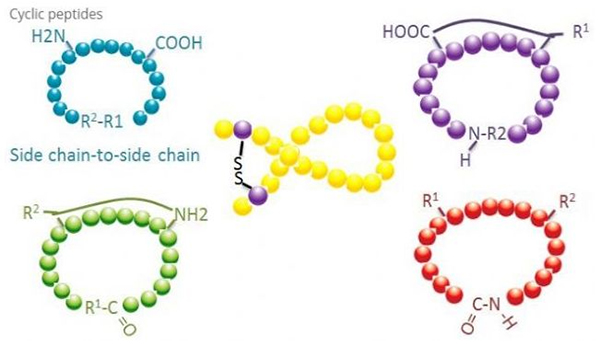
(2) термінал-бічний ланцюг
Циклізація кінцевого бічного ланцюга зазвичай включає С-кінець з аміногрупою бічного ланцюга лізину або орнітину або N-кінець з бічним ланцюгом аспарагінової кислоти або глутамінової кислоти.Інша поліпептидна циклізація здійснюється шляхом утворення ефірних зв’язків між кінцевим C і бічними ланцюгами серину або треоніну.
(3) Термінальний або тип «голова до хвоста».
Ланцюгові поліпептиди можна циклізувати в розчиннику або фіксувати на смолі за допомогою циклювання бічного ланцюга.Низькі концентрації пептидів слід використовувати для централізації розчинника, щоб уникнути олігомеризації пептидів.Вихід синтетичного кільцевого поліпептиду типу «голова-хвіст» залежить від послідовності ланцюга поліпептиду.Таким чином, перш ніж готувати циклічні пептиди у великому масштабі, спочатку слід створити бібліотеку можливих ланцюгових провідних пептидів з подальшою циклізацією, щоб знайти послідовність з найкращими результатами.
2. N-метилювання
N-метилювання спочатку відбувається в природних пептидах і вводиться в синтез пептидів, щоб запобігти утворенню водневих зв’язків, тим самим роблячи пептиди більш стійкими до біодеградації та очищення.Найважливішим методом є синтез пептидів з використанням похідних N-метильованих амінокислот.Крім того, також можна використовувати реакцію Міцунобу проміжних продуктів N-(2-нітробензолсульфонілхлорид) поліпептид-смола з метанолом.Цей метод був використаний для отримання бібліотек циклічних пептидів, що містять N-метильовані амінокислоти.
3. Фосфорилювання
Фосфорилювання є однією з найпоширеніших посттрансляційних модифікацій у природі.У клітинах людини фосфорильовано понад 30% білків.Фосфорилювання, особливо оборотне фосфорилювання, відіграє важливу роль у контролі багатьох клітинних процесів, таких як трансдукція сигналу, експресія генів, регуляція клітинного циклу та цитоскелету, а також апоптоз.
Фосфорилювання можна спостерігати за різними амінокислотними залишками, але найпоширенішими мішенями фосфорилювання є залишки серину, треоніну та тирозину.Похідні фосфотирозину, фосфотреоніну та фосфосерину можуть бути введені в пептиди під час синтезу або утворені після синтезу пептидів.Селективного фосфорилювання можна досягти за допомогою залишків серину, треоніну та тирозину, які вибірково видаляють захисні групи.Деякі реагенти фосфорилювання також можуть вводити групи фосфорної кислоти в поліпептид шляхом пост-модифікації.В останні роки сайт-специфічне фосфорилювання лізину було досягнуто за допомогою хімічно селективної реакції Штаудінгера-фосфіту (рис. 3).
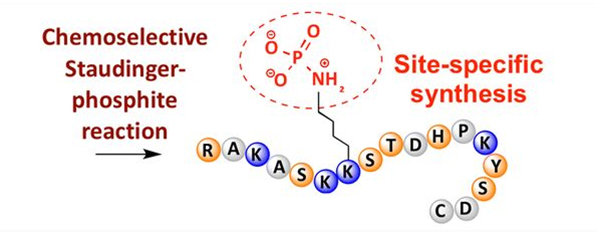
4. Мірістоїлування та пальмітоїлування
Ацилювання N-кінца жирними кислотами дозволяє пептидам або білкам зв'язуватися з клітинними мембранами.Міридамоїльована послідовність на N-кінці дає можливість протеїнкіназам родини Src і білкам зворотної транскриптази Gaq націлюватися на зв’язування з клітинними мембранами.Міристинова кислота була зв'язана з N-кінцем поліпептиду-смола за допомогою стандартних реакцій сполучення, і отриманий ліпопептид міг бути дисоційований за стандартних умов і очищений за допомогою ВЕРХ з обертовою фазою.
5. Глікозилювання
Такі глікопептиди, як ванкоміцин і тейколанін, є важливими антибіотиками для лікування резистентних бактеріальних інфекцій, а інші глікопептиди часто використовуються для стимуляції імунної системи.Крім того, оскільки багато мікробних антигенів є глікозильованими, велике значення має вивчення глікопептидів для покращення терапевтичного ефекту інфекції.З іншого боку, було виявлено, що білки на клітинній мембрані пухлинних клітин демонструють аномальне глікозилювання, що робить глікопептиди відіграють важливу роль у дослідженнях імунного захисту раку та пухлин.Глікопептиди отримують методом Fmoc/t-Bu.Глікозильовані залишки, такі як треонін і серин, часто вводяться в поліпептиди fMOCs, активованими ефіром пентафторфенолу, для захисту глікозильованих амінокислот.
6. Ізопрен
Ізопентадієнілювання відбувається на залишках цистеїну в бічному ланцюзі біля С-кінца.Протеїновий ізопрен може покращувати спорідненість клітинної мембрани та формувати білок-білкову взаємодію.Ізопентадієновані білки включають тирозинфосфатазу, малу ГТазу, молекули кохаперону, ядерну пластинку та центромерні зв’язувальні білки.Ізопренові поліпептиди можуть бути отримані з використанням ізопрену на смолах або шляхом введення похідних цистеїну.
7. Модифікація поліетиленгліколю (ПЕГ).
Модифікація PEG може бути використана для покращення гідролітичної стабільності білка, біорозподілу та розчинності пептиду.Введення ланцюгів ПЕГ до пептидів може покращити їх фармакологічні властивості, а також пригнічувати гідроліз пептидів протеолітичними ферментами.Пептиди PEG проходять крізь поперечний зріз капілярів клубочків легше, ніж звичайні пептиди, значно знижуючи нирковий кліренс.Завдяки подовженому активному періоду напіврозпаду пептидів PEG in vivo нормальний рівень лікування можна підтримувати меншими дозами та менш частими пептидними препаратами.Однак модифікація PEG також має негативні наслідки.Великі кількості ПЕГ перешкоджають ферменту руйнувати пептид, а також зменшують зв’язування пептиду з цільовим рецептором.Але низька спорідненість пептидів ПЕГ зазвичай компенсується їх довшим фармакокінетичним періодом напіврозпаду, і, будучи присутніми в організмі довше, пептиди ПЕГ мають більшу ймовірність всмоктування в цільові тканини.Тому специфікації ПЕГ полімеру повинні бути оптимізовані для отримання оптимальних результатів.З іншого боку, пептиди PEG накопичуються в печінці через знижений нирковий кліренс, що призводить до макромолекулярного синдрому.Тому модифікації ПЕГ необхідно розробляти більш ретельно, коли пептиди використовуються для тестування ліків.
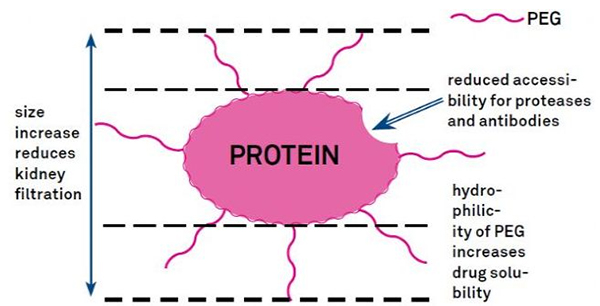
Загальні модифікаційні групи модифікаторів PEG можна приблизно узагальнити таким чином: аміно (-амін) -NH2, амінометил-Ch2-NH2, гідрокси-OH, карбокси-Cooh, сульфгідрил (-тіол) -SH, малеімід -MAL, сукцинімід карбонат - SC, сукцинімід ацетат -SCM, сукцинімід пропіонат -SPA, n-гідроксисукцинімід -NHS, акрилат-ch2ch2cooh, альдегід -CHO (такий як пропіонал-альд, бутирALD), акрилова основа (-акрилат-acrl), азидо-азид, біотиніл - Біотин, флуоресцеїн, глутарил -GA, акрилатгідразид, алкін-алкін, п-толуолсульфонат -OTs, сукцинімід сукцинат -SS тощо. Похідні PEG з карбоновими кислотами можуть бути з'єднані з n-кінцевими амінами або бічними ланцюгами лізину.Аміно-активований ПЕГ може бути приєднаний до бічних ланцюгів аспарагінової кислоти або глутамінової кислоти.Порушено активований ПЕГ може бути кон’югований з меркаптаном із повністю знятими захистом бічних ланцюгів цистеїну [11].Модифікатори PEG зазвичай класифікуються таким чином (примітка: mPEG – це метокси-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) модифікатор PEG з прямим ланцюгом
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) біфункціональний модифікатор PEG
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) модифікатор ПЕГ розгалуження
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Біотинізація
Біотин може міцно зв'язуватися з авідином або стрептавідином, і сила зв'язування навіть близька до ковалентного зв'язку.Пептиди, мічені біотином, зазвичай використовуються в імунологічному аналізі, гістоцитохімії та проточній цитометрії на основі флуоресценції.Мічені антитіла до антибіотину також можна використовувати для зв'язування біотинільованих пептидів.Мітки біотину часто прикріплюються до бічного ланцюга лізину або N-кінці.6-амінокапронова кислота часто використовується як зв'язок між пептидами та біотином.Зв'язок гнучкий у зв'язуванні з субстратом і краще зв'язується за наявності стеричних перешкод.
9. Флуоресцентне маркування
Флуоресцентне мічення можна використовувати для відстеження поліпептидів у живих клітинах і для вивчення ферментів і механізмів дії.Триптофан (Trp) є флуоресцентним, тому його можна використовувати для внутрішнього маркування.Спектр випромінювання триптофану залежить від периферійного середовища та зменшується зі зменшенням полярності розчинника, властивість, корисна для виявлення структури пептиду та зв’язування рецептора.Флуоресценцію триптофану можна погасити протонованою аспарагіновою кислотою та глутаміновою кислотою, що може обмежити його використання.Хлоридна група Дансил (Dansyl) сильно флуоресцентна, коли зв’язана з аміногрупою, і часто використовується як флуоресцентна мітка для амінокислот або білків.
Флуоресцентне резонансне перетворення енергії (FRET) корисне для дослідження ферментів.Коли застосовується FRET, субстратний поліпептид зазвичай містить групу для мічення флуоресценції та групу для гасіння флуоресценції.Мічені флуоресцентні групи гасяться гасником шляхом нефотонної передачі енергії.Коли пептид відокремлюється від відповідного ферменту, група мічення випромінює флуоресценцію.
10. Кліткові поліпептиди
Кліткові пептиди мають оптично видаляються захисні групи, які захищають пептид від зв’язування з рецептором.Під дією УФ-випромінювання пептид активується, відновлюючи свою спорідненість з рецептором.Оскільки цю оптичну активацію можна контролювати відповідно до часу, амплітуди або місця, кліткові пептиди можна використовувати для вивчення реакцій, що відбуваються в клітинах.Найбільш часто використовуваними захисними групами для клітинних поліпептидів є 2-нітробензильні групи та їх похідні, які можуть бути введені в пептидний синтез за допомогою захисних похідних амінокислот.Похідними амінокислот, які були розроблені, є лізин, цистеїн, серин і тирозин.Однак похідні аспартату та глутамату зазвичай не використовуються через їх схильність до циклізації під час синтезу та дисоціації пептидів.
11. Поліантигенний пептид (MAP)
Короткі пептиди зазвичай не мають імунітету і повинні бути з’єднані з білками-носіями для виробництва антитіл.Поліантигенний пептид (MAP) складається з кількох ідентичних пептидів, з’єднаних з ядрами лізину, які можуть специфічно експресувати високопотенційні імуногени та можуть бути використані для приготування куплетів білок-носій пептид.Поліпептиди MAP можна синтезувати шляхом твердофазного синтезу на смолі MAP.Однак неповне з’єднання призводить до відсутності або усічення пептидних ланцюгів на деяких гілках і, таким чином, не демонструє властивостей оригінального поліпептиду MAP.Як альтернатива, пептиди можуть бути отримані та очищені окремо, а потім з'єднані з MAP.Пептидна послідовність, приєднана до пептидного ядра, чітко визначена і легко визначається за допомогою мас-спектрометрії.
Висновок
Модифікація пептидів є важливим засобом конструювання пептидів.Хімічно модифіковані пептиди можуть не тільки підтримувати високу біологічну активність, але й ефективно уникати таких недоліків, як імуногенність і токсичність.У той же час хімічна модифікація може наділити пептиди новими чудовими властивостями.В останні роки метод активації СН для постмодифікації поліпептидів був швидко розроблений, і було досягнуто багато важливих результатів.
Час публікації: 20 березня 2023 р
